شناساگر اسید و باز (معرف PH) چیست؟: (عملکرد، انواع و کاربردها)
- تعاریف شیمی, تجهیزات و لوازم آزمایشگاهی, علم شیمی, کاربردهای شیمی
- ۱۴۰۳/۱۲/۲۲

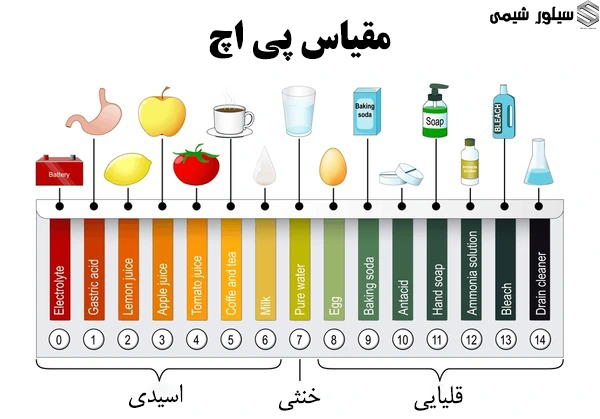
در دنیای شیمی، تشخیص اسیدها و بازها از اهمیت زیادی برخوردار است. تعداد زیادی از مواد شیمیایی با حل شدن در آب، آب را به اسید یا باز تبدیل میکنند(محلول بازی دارای PH>7 و محلول اسیدی دارای PH<7 است).
بسیاری از اسیدها و بازها در حالت خالص بیرنگ هستند و تشخیص آنها با چشم غیرمسلح ممکن نیست. برای حل این مشکل، از موادی به نام شناساگرهای اسید و باز یا همان معرفهای pH استفاده میشود. شناساگرهای اسید و باز، ترکیبات شیمیایی خاصی هستند که به تغییر غلظت یونهای هیدروژن (⁺H) در محیط حساساند و در محیطهای اسیدی و بازی تغییر رنگ میدهند. این مواد، با تغییر رنگ خود، اطلاعاتی درباره میزان اسیدی یا بازی بودن یک محلول ارائه میدهند. شناساگرها به عنوان ابزاری ساده و مؤثر در شیمی تحلیلی، آزمایشگاهها، صنایع و حتی مصارف خانگی مورد استفاده قرار میگیرند.
📒 در این مقاله، به بررسی مفهوم شناساگرهای اسید و باز، نحوه عملکرد آنها، انواع مختلف و کاربردهایشان خواهیم پرداخت.
شناساگر اسید و باز چیست؟
شناساگر اسید و باز (pH indicator) یک ترکیب شیمیایی هالوکرومیک است که در محیطهای مختلف pH تغییر رنگ میدهند و میتوانند میزان اسیدی یا بازی بودن یک محلول را مشخص کنند. این تغییر رنگ به دلیل تغییر ساختار مولکولی آنها در حضور یونهای ⁺H و ⁻OH است. شناساگر اسید و باز در حقیقت اسید یا باز ضعیفی است که بین شکل یونی و مولکولی آن تعادلی برقرار است و با تغییر میزان غلظت +H یا -OH تغییر رنگ می دهد. این معرف ها بسته به نوعشان، در محدودههای مختلفی از پی اچ تغییر رنگ میدهند. برخی از این شناساگرها ترکیبات طبیعی مانند آنتوسیانینهای موجود در گلبرگها و میوهها هستند، در حالی که برخی دیگر بهصورت مصنوعی ساخته شدهاند و کاربردهای گستردهای در شیمی تجزیه و آزمایشهای علمی دارند.
📌 این مواد رقیق هستند و بر روی pH واکنش تاثیر نمی گذارند.
شناساگرهای اسید و باز به طور معمول در فرآیند تیتراسیون کاربرد دارند و به کمک آنها میتوان نقطه پایانی یک واکنش اسید و باز را مشخص کرد(در نزدیکی نقطه تعادل در اثر تغییر غلظت مواد تیترشونده شروع به تغییر رنگ میکند).

عملکرد شناساگر اسید و باز چگونه است؟
شناساگرهای pH ترکیبات آلی ضعیف (اسیدی یا بازی) هستند که در محیطهای اسیدی و بازی ساختار مولکولی آنها تغییر کرده و در نتیجه رنگشان تغییر میکند. این تغییر رنگ به دلیل واکنش تعادلی بین گونههای یونی و غیریونی آنهاست. برای مثال متیل اورانژ در محلولهای آبی با PH های کمتر از 3.۱ رنگ آن به قرمز نزدیک میشود و برای PH های ۳.۱ و بیشتر از آن، زرد رنگ میشود. موادی مثل متیل اورانژ که از آنها برای تعیین pH محلولها استفاده میشود، شناساگر اسید و باز ( معرف اسید و باز ) هستند.
🧬 فرمول عملکرد متیل اورانژ:
متیل اورانژ (اسید ضعیف) در محیط اسیدی به رنگ قرمز و در محیط بازی به رنگ زرد دیده میشود. این تغییر به واسطه واکنش تعادلی زیر اتفاق میافتد:
HIn(aq) + H۲O(l) ⇌ H۳O+(aq)+ In–(aq)
💡راهنما:
متیل اورانژ = HIn (شکل یونیزه نشده) ⬅ رنگ: قرمز
آب = H۲O
یون هیدرونیوم = +H۳O
آنیون متیل اورانژ = –In (شکل یونیزه شده) ⬅ رنگ: زرد
۱- بررسی حالتها از روش غیر فرمولی:
۱- اگر اسیدی به محلول متیل اورانژ اضافه شود، به دلیل افزایش یون هیدرونیوم، برای اینکه تعادل واکنش حفظ شود واکنش به سمت چپ میرود و غلظت HIn زیاد شده و رنگ محلول به سمت قرمز میرود (بستگی به مقدار اسید دارد).
۲- اگر بازی به محلول متیل اورانژ اضافه شود، با یون هیدرونیوم واکنش داده و آن را به آب خنثی تبدیل میکند. برای اینکه تعادل واکنش حفظ شود و جای یون هیدرونیوم مصرف شده جبران شود واکنش به سمت راست جا به جا میشه و غلظت آنیون متیل اورانژ افزایش مییابد و رنگ محلول به زرد نزدیک میشود (بستگی به مقدار باز دارد).
💡 این رفتار شبیه به رفتار محلول های بافر میباشد:
برای سفارش انواع محلول های بافر از فروشگاه سیلور شیمی بازدید کنید:
• در محیط اسیدی (pH پایین)، فرم غیر یونیزهشده (HIn) رنگ قرمز دارد.
• در محیط بازی (pH بالا)، فرم یونیزهشده (⁻In) رنگ زرد دارد.
۲- بررسی حالتها از روش فرمولی: (مطالعه تخصصی تر)
ابتدا بیایید ثابت تفکیک اسید را برای معادله متیل اورانژ بنویسیم:
Ka= ( [H۳O+] [In–] )/( [HIn] ) = 4×۱۰-۴
شکل دیگر فرمول:
( [HIn] /[–In] ) = ( [+H۳O]/ [Ka])
۱- زمانی که مقدار عددی غلظت +H۳O و Ka برابر باشد یعنی غلظت HIn (قرمز) برابر غلظت –In (زرد) است به عبارتی به صورت مساوی ترکیبی از رنگ قرمز و زرد را داریم که به معنی رنگ نارنجی است.
۲- زمانی که مقدار یون هیدرونیوم زیاد شود، مقدار HIn (قرمز) زیاد میشود و محلول به سمت رنگ قرمز میرود.
۳- اگر مقدار یون هیدرونیوم کم شود، مقدار –In (زرد) زیاد میشود و محلول به سمت رنگ زرد میرود.
PH بین ۳.۱ و ۴.۴ بازه کاربردی تغییر رنگ(🟨⇌🟥) متیل اورانژ است.
‼بعضی از این شناساگر ها از رنگی به رنگ دیگر و برخی از بی رنگ به رنگی شدن و یا رنگی به بیرنگ شدن تبدیل میشوند.
چرا از شناساگر اسید و باز استفاده میکنیم؟
اسید و باز در دنیای مواد شیمیایی نقش کلیدی دارند؛ به طوری که استفاده از آنها در دنیای شیمی فراوان است. بنابراین شناسایی این ترکیبات بسیار مهم است و همینطور از نظر شکل ظاهری هم تقریبا مشابه یکدیگراند (بسیاری از اسیدها و بازها در حالت خالص بیرنگ هستند).
البته اسیدها و بازها مزه متفاوتی دارند ( اسید = ترش – باز = تلخ) ولی از آنجایی که اغلب این ترکیبات خواص خوردنگی دارند، باعث سوختگی و از بین رفتن بافت های بدن میشوند. پس نمیتوان آنها را مزه کرد❌.
شناساگر ها با تغییر رنگ محلول، میزان اسیدی یا بازی بودن محلول ها را مشخص می کنند؛ بنابراین استفاده از این معرف ها در آزمایشگاه ها و… امری طبیعی است.
ویژگیهای یک معرف PH
✅ تغییر رنگ سریع و مشخص:
شناساگر باید در محدوده pH خاص خود، تغییر رنگ قابل مشاهده و سریعی داشته باشد.
✅ حساسیت بالا:
مقدار کمی از آن باید برای تشخیص کافی باشد.
✅ عدم تأثیرگذاری بر واکنش شیمیایی:
نباید با مواد دیگر (ماده تحت تیتراسیون) واکنش دهد.
✅ پایداری شیمیایی مناسب:
در طول زمان یا تحت شرایط مختلف تغییر ماهیت ندهد یا از بین نرود.
✅ غیرسمی و ایمن باشد:
برای استفاده در محیطهای مختلف مناسب باشد.
✅ کمترین خطا را داشته باشد:
مقدار دامنه pK شناساگر باید در بازه ۱ واحدی از مقدار pH مورد انتظار نقطه تعادل (همارزی) قرار داشته باشد.
‼شناساگرهای سنتزی تولید شدهاند که همه شرایط بالا را دارند و به کمک آنها میتوان دامنه وسیعی از PH را در برگرفت. برخی از معرفها همچون تیمول آبی، اسیدهایی چند پروتونه (بیش از یک هیدروژن اسیدی دارند) هستند که رنگ آن دو بار در دو محدوده مختلف تغییر میکند.
انواع شناساگرها
شناساگرها به دو دسته کلی تقسیم میشوند:
۱- شناساگرهای داخلی:
این شناساگرها درون محلول حل شده و تغییر رنگ آن را نشان میدهند. به طور مثال اگر به محلول تیتر شونده، چند قطره از یک معرف اضافه شود، پس از پایان، تغییر رنگ در محلول ایجاد میشود. مثالها:
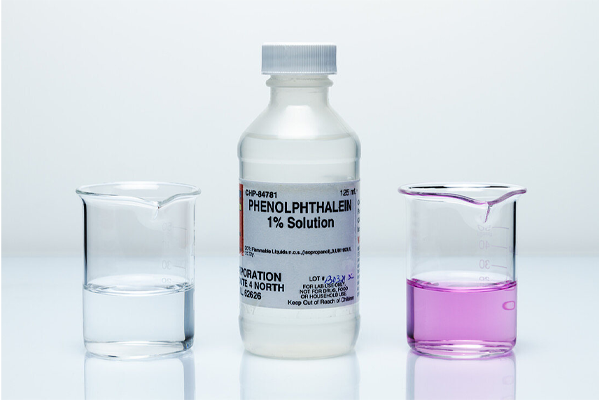
◼ فنل فتالئین
◼ متیل اورانژ
◼ برمو تیمول بلو
۲. شناساگرهای خارجی (pH متر و نوارهای pH)
این شناساگرها روی نوارهای خاصی آغشته شدهاند و هنگام تماس با محلول تغییر رنگ میدهند.(بدون تغییر در ترکیب محلول، میزان pH را اندازهگیری میکنند) مانند کاغذ تورنسل.
⬅ مثال: در برخی حالات قبل از آن که نقطه پایان پدیدار شود، بین شناساگر و محلول تیتر شونده یک واکنش صورت میگیرد و در این حالت نقطه پایان سریعتر اتفاق میافتد، مثل تیتر کردن فسفات با استات اورانیل در حضور معرف فروسیانور پتاسیم؛ فروسیانور پتاسیم با یونهای اورانیل قبل از رسیدن به نقطه پایان واکنش میدهد. برای بدست آوردن نتیجه مناسب باید به دفعات مورد نیاز چند قطره از محلولی که پس از صاف کردن رسوب بدست میآید را در فاصله زمانی مساوی، روی یک قطعه کاغذ صافی با معرف سیانور پتاسیم آزمایش کرد.
⬅ از نمایی دیگر: شاخص های پی اچ به صورت مایع و کاغذی موجود هستند. شکل مایع آن ها به محلول اضافه می شود، در حالی که شکل کاغذی آن را چند ثانیه درون محلول نگه میدارند و بعد آن را با راهنمای رنگی مقایسه می کنند تا از تغییر رنگ کاغذ بتوان مقدار PH را اندازه گیری نمود.

معروفترین شناساگرهای اسید و باز
۱- متیل اورانژ (متیل نارنجی):
این معرف جزو یکی از پرکاربردترین شناساگرها است و معمولاً در تیتراسیون به همراه اسید و برای شناسایی بازها مورد استفاده قرار می گیرد. این شناساگر در برخورد با اسید به رنگ قرمز 🟥 و در برخورد با محیط های قلیایی زرد 🟨 میشود.
✅ محدوده PH کاربردی این شناساگر بین ۳.۱ – ۴.۴ است.

۲- فنل فتالئین:
این معرف در تیتراسیون و به جهت تعیین محلول های اسیدی مورد استفاده قرار می گیرد. فنل فتالئین ترکیبی از خانواده فتالئینها است. فنل فتالئین در حالت عادی و محیط های اسیدی بی رنگ بوده و در محدوده پی اچ ۸.۵ تا ۱۰ (محلول های قلیایی) رنگی صورتی دارد.
✅ محدوده PH کاربردی این شناساگر بین ۸ – ۱۰ است.
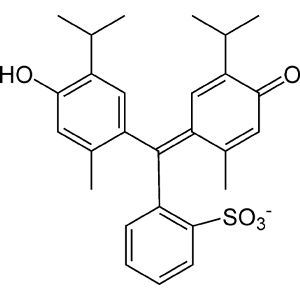
۳- تیمول بلو:
تیمول بلو (تیمو سولفو نفتالئین) معرفی با رنگ قهوه ای است.
✅ اولین انتقال رنگی: تغییر پی اچ ۱.۲ – ۲.۸ به رنگ زرد 🟨 تبدیل میشود.
✅ دومین انتقال رنگی: تغییر پی اچ ۸ – ۹.۶ به رنگ آبی 🟦 در میآید.
۴- بروموکروزول سبز:
سبز بروموکروزول (BCG) در تیتراسیون های اسید و باز، رشد میکروبیولوژیکی، و الکتروفورز ژل آگارز برای جداسازی DNA به کار می رود.
در PH های کمتر از ۳.۸ محلول زرد رنگ 🟨 خواهد بود و در pH=5.4 و بالاتر محلول آبی رنگ 🟦 است و در PH بین ۳.۸ و ۵.۴ سبز رنگ 🟩 است.
✅ محدوده PH کاربردی این شناساگر بین ۳.۸ – ۵.۴ است.

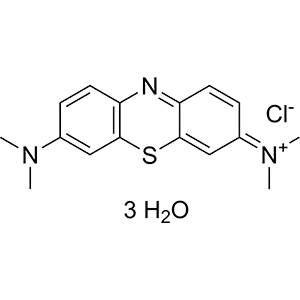
۵- متیلن بلو:
متیلن بلو یک ترکیب شیمیایی معطر هتروسیکلیک با فرمول مولکولی C۱۶H۱۸N۳SCl است. متیل بلو در واکنش های اکسایش – کاهش مورد استفاده قرار می گیرد و در دمای اتاق پودری جامد و سبز تیره رنگ است که وقتی در آب حل شود محلولی آبی رنگ میشود.
متیلن بلو آبی رنگ در صورتی که در واکنش، عملیات احیا انجام شود به سمت بی رنگ شدن میرود و در صورتی که در واکنش مجددا اکسید شدن اتفاق بیوفتد، متیلن بلو مجددا می تواند به رنگ آبی 🟦 تبدیل شود.
۶- یونیورسال (Universal Indicator):
رنگهای مختلف برای محدودههای مختلف pH را نشان میدهد.
‼برای هر شناساگر دامنه PH ویژه ای تعریف شده است که باید با اطلاع از دامنه های تغییر رنگ، معرف مناسب برای آزمایش موردنظر را انتخاب کنیم.

برای سفارش نوار تست PH یونیورسال کلیک کنید:
شناساگر اسید و باز طبیعی
در طبیعت گیاهان زیادی وجود دارند که با تغییر رنگ در محیط های اسیدی و بازی میتوانند به عنوان شناساگر فعالیت کنند. شناساگرهای طبیعی از گیاهان دارای ترکیبات رنگی خانواده آنتوسیانین هستند و در محیطهای اسیدی به رنگ قرمز 🟥 و بازی به بنفش و آبی 🟦🟪 تغییر رنگ میدهند.
⬅ مثال: لیتموس (Litmus) یکی از قدیمیترین و پرکاربردترین شناساگرهای اسید و باز است که از یک منبع طبیعی به دست میآید. این شناساگر از رنگدانههای استخراجشده از گلسنگها (Lichens)، بهویژه گونههایی از جنس Roccella و Lecanora تهیه میشود.
📌 رنگ لیتموس در محیطهای مختلف:
لیتموس در محیط اسیدی به رنگ قرمز 🟥 و در محیط های بازی به رنگ آبی 🟦 است.
📌 عملکرد لیتموس:
لیتموس در واقع یک رنگدانه آلی است که تحت تأثیر یونهای هیدروژن (+H) و یونهای هیدروکسید (-OH) ساختار شیمیاییاش تغییر کرده و در نتیجه رنگ متفاوتی نشان میدهد.
📌 موارد استفاده از لیتموس:
• نوار لیتموس، بهعنوان یک کاغذ تست سریع برای تشخیص اسیدی یا بازی بودن محلولها به کار میرود.
• محلول لیتموس، در آزمایشگاهها برای بررسی pH استفاده میشود.
📌 مزیتهای لیتموس:
• طبیعی و غیرسمی است.
• استفاده آسان و پاسخدهی سریع دارد.
• در آزمایشگاهها، مدارس و صنایع بهعنوان یک روش ساده برای تعیین pH استفاده میشود.

نمونه هایی از شناساگرهای طبیعی
| شناساگر | pH اسیدی | pH بازی |
|---|---|---|
| زردچوبه | زرد | قهوهای |
| گل ادریسی | آبی | صورتی تا بنفش |
| لیتموس | قرمز | آبی |
| کلم قرمز | قرمز | سبز و آبی |
| چای سیاه | زرد | قهوهای |
| گلبرگ گل رز | قرمز | آبی |
| چغندر | قرمز تیره | زرد |
| زغالاخته | قرمز | بنفش تا سبز |
به چه شناساگرهایی شناساگر جهانی میگویند؟
شناساگرهای جهانی ترکیبی از چند شناساگر هستند که در طیف گستردهای از pH تغییر رنگ میدهند.
⬅ مثال ۱: از ترکیب متیل اورانژ، تیمول بلو، فنل فتالئین و برموتیمول بلو، معرف یونیورسال ساخته شده است.
⬅ مثال ۲: از ترکیب تیمول آبی، متیل قرمز، برموتیمول بلو و فنل فتالئین می توان شناساگری با دامنه ی pH کمتر از ۳ با رنگ قرمز 🟥 و بالاتر از ۱۱ با رنگ بنفش 🟪 ایجاد کرد. پی اچ ۳ تا ۶ با رنگ نارنجی/زرد 🟧🟨، پی اچ ۷ با رنگ سبز 🟩 ، پی اچ ۸ تا ۱۱ با رنگ آبی 🟦.
شناساگرهای جهانی معمولاً به صورت کاغذ pH هستند.
⁉ تفاوت شناساگر جهانی با کاغذ لیتموس:
شناساگر جهانی می تواند به طور تقریبی pH واکنش را با کمک جدول راهنما پیدا کند، ولی کاغذ لیتموس فقط می تواند اسیدی یا بازی بودن محیط واکنش را تشخیص دهد.
برای سفارش شناساگر جهانی PH با برند مرک آلمان کلیک کنید:
انواع کاربردهای شناساگر اسید و باز
۱. کاربرد در آزمایشگاههای شیمی
شناساگرهای اسید و باز یکی از ابزارهای اصلی در آزمایشگاههای شیمی هستند و در انجام واکنشهای مختلف، کنترل فرآیندهای شیمیایی و تعیین اسیدی یا بازی بودن محلولها استفاده میشوند. مهمترین موارد استفاده در آزمایشگاه شامل:
• تعیین pH محلولها: با استفاده از شناساگرهای طبیعی یا مصنوعی مانند فنل فتالئین، متیل اورانژ، لیتموس و یونیورسال.
• تیتراسیونهای اسید و باز: در تیتراسیونهای شیمیایی، از شناساگرهایی مانند فنل فتالئین و متیل اورانژ برای تعیین نقطه پایانی واکنش استفاده میشود.
• تشخیص ترکیبات ناشناخته: برخی ترکیبات در محیطهای اسیدی یا بازی خاص تغییر رنگ داده و به شناسایی آنها کمک میکنند.

۲. کاربرد در پزشکی و داروسازی
شناساگرهای اسید و باز نقش مهمی در صنایع داروسازی و پزشکی دارند. برخی از کاربردهای مهم در این زمینه شامل:
• تعیین سطح اسیدیته خون و ادرار: در آزمایشهای پزشکی، از نوارهای شناساگر برای بررسی pH خون، ادرار و سایر مایعات بدن استفاده میشود.
• کنترل فرمولاسیون داروها: بسیاری از داروها باید در pH خاصی تهیه شوند تا اثرگذاری بهتری داشته باشند. شناساگرهای pH، برای تنظیم محیط دارویی کاربرد دارند.
• بررسی میزان اسیدیته معده: در پزشکی از شناساگرها برای بررسی میزان اسید معده و تشخیص بیماریهایی مانند رفلاکس معده استفاده میشود.
۳. استفاده در صنایع غذایی
در صنایع غذایی، pH مواد خوراکی تأثیر مستقیمی بر کیفیت، طعم، ایمنی و ماندگاری محصولات دارد. برخی از کاربردهای مهم شناساگرهای اسید و باز در این صنعت شامل:
• کنترل کیفیت مواد غذایی: تعیین میزان اسیدی یا بازی بودن مواد غذایی برای جلوگیری از فساد.
• بررسی تازگی محصولات لبنی: در محصولات لبنی مانند شیر، تغییر pH میتواند نشاندهنده فاسد شدن آن باشد.
• فرآوری و نگهداری غذاها: برخی مواد غذایی نیاز به تنظیم pH دارند تا عمر ماندگاری بیشتری داشته باشند (مانند تولید کنسروها).
• تعیین میزان اسیدیته نوشیدنیها: نوشیدنیهایی مانند نوشابه، آبمیوهها و چای دارای pH مشخصی هستند که با استفاده از شناساگرها کنترل میشود.
۴. کاربرد در تصفیه آب و محیط زیست
شناساگرهای pH در کنترل و پایش کیفیت آب و محیط زیست اهمیت زیادی دارند. برخی از کاربردهای مهم آنها در این زمینه عبارتاند از:
• بررسی کیفیت آب آشامیدنی: اندازهگیری pH آب برای اطمینان از سالم بودن آن.
• کنترل آلودگی صنعتی: فاضلابهای صنعتی ممکن است اسیدی یا بازی باشند و باید قبل از ورود به محیطزیست، خنثی شوند.
• کنترل فرآیند تصفیه آب: در فرآیندهای تصفیه آب، pH نقش مهمی در حذف آلودگیها و تهنشینی مواد دارد.
۵. کاربرد در کشاورزی و خاکشناسی
شناساگرهای pH در کشاورزی برای بررسی میزان اسیدیته و قلیاییت خاک استفاده میشوند. pH خاک یکی از عوامل مهم در رشد گیاهان است و بر جذب مواد مغذی تأثیر میگذارد. برخی از کاربردها شامل:
• بررسی pH خاک و کود: تعیین میزان اسیدی یا بازی بودن خاک برای تنظیم نوع کود و شرایط کشت.
• کنترل کیفیت آب آبیاری: بررسی pH آب آبیاری برای جلوگیری از آسیب به گیاهان.
• بهینهسازی شرایط رشد گیاهان: برخی گیاهان در خاکهای اسیدی یا قلیایی بهتر رشد میکنند و تنظیم pH به بهبود عملکرد محصول کمک میکند.
۶. استفاده در صنایع آرایشی و بهداشتی
pH محصولات آرایشی و بهداشتی تأثیر زیادی بر سلامت پوست و مو دارد. تنظیم مناسب pH در تولید این محصولات از اهمیت بالایی برخوردار است. برخی از کاربردهای مهم:
• تعیین pH محصولات مراقبت از پوست و مو: شامپوها، کرمها و صابونها باید در pH مناسب تهیه شوند تا به پوست آسیب نزنند.
• کنترل کیفیت مواد آرایشی: pH برخی مواد آرایشی برای جلوگیری از ایجاد حساسیتهای پوستی تنظیم میشود.
• بررسی pH صابونها و شویندهها: برای جلوگیری از ایجاد خشکی و تحریک پوست.
۷. استفاده در صنایع کاغذ، رنگ و نساجی
در این صنایع، کنترل pH در فرآیندهای مختلف تولید و رنگرزی اهمیت زیادی دارد.
• کنترل pH در تولید کاغذ: تنظیم میزان اسیدی یا بازی بودن خمیر کاغذ برای افزایش کیفیت.
• کنترل pH در صنعت رنگرزی: رنگهای مختلف در محیطهای اسیدی یا بازی رفتار متفاوتی دارند و pH مناسب باعث بهبود رنگ و ثبات آن روی پارچه میشود.
• کنترل pH در تولید رنگ و جوهر: برخی رنگها و جوهرها در pH خاصی بهترین عملکرد را دارند.
۸. تولید و بررسی مواد شیمیایی
شناساگرهای pH در صنایع شیمیایی برای بررسی خلوص و کنترل کیفیت مواد شیمیایی کاربرد دارند.
• کنترل pH در تولید مواد شیمیایی صنعتی: برخی واکنشهای شیمیایی نیاز به محیط اسیدی یا بازی خاصی دارند.
• استفاده در فرمولاسیون محصولات شیمیایی: برای تنظیم pH در تولید مواد شوینده، ضدعفونیکنندهها و محصولات دیگر.
انجام آزمایش و تهیه شناساگر برای درک بهتر
درباره شناساگرهای طبیعی که یکی از آنها کلم قرمز بود صحبت کردیم و گفتیم در محیط های مختلف چه رنگی دارند، حالا وقتش هست بریم سراغ تولید یکی از این شناساگرهای طبیعی.
🧫 تهیه شناساگر طبیعی از کلم قرمز:
مواد لازم:
◼ برگ کلم قرمز
◼ دیگچه
◼ کاغذ صافی
◼ آمونیاک یا جوش شیرین (باز)
◼ سرکه (اسید)
◼ آب
روش کار:
۱- برگهای کلم را خرد و درون دیگچه بگذارید و آنها را از آب بپوشانید.
۲- ۳۰ دقیقه آنها را با شعله ی ملایم بجوشانید.
‼به جای مراحل ۱ و ۲ میتوان از مخلوط کن استفاده کرد.
۳- اجازه دهید کلم ها خنک شوند و آن ها را از صافی عبور دهید.
۴- آب کلم را به دو ظرف مجزا بریزید، به یک ظرف سرکه می افزاییم و به ظرف دیگر آمونیاک.
۵- رنگها در محیط اسیدی قرمز 🟥 و در محیط بازی تغییر رنگ از بنفش به سبز (🟪⬅🟩) خواهد بود.
فیلم آموزشی تهیه شناساگر طبیعی از کلم قرمز
رعایت نکات ایمنی در استفاده از شناساگرها
برخی از این مواد ممکن است سمی، خورنده یا تحریککننده باشند، بنابراین رعایت نکات ایمنی هنگام کار با آنها ضروری است.
⚠ استفاده از تجهیزات ایمنی مناسب:
• دستکش محافظ: برخی شناساگرهای شیمیایی میتوانند باعث تحریک پوست شوند، بنابراین دستکش نیتریل یا لاتکس استفاده کنید.
• عینک ایمنی: برای محافظت از چشمها در برابر پاشش احتمالی محلولهای اسیدی یا قلیایی.
• ماسک یا تهویه مناسب: هنگام کار با شناساگرهایی که بخارات سمی تولید میکنند (مانند فنل فتالئین یا تیمول بلو)، حتماً در محیط با تهویه مناسب کار کنید یا ماسک بزنید.
• پوشش آزمایشگاهی: برای جلوگیری از تماس محلولها با لباس و پوست، از روپوش آزمایشگاهی استفاده کنید.
⚠ رعایت اصول نگهداری و ذخیرهسازی صحیح:
• دور از نور مستقیم خورشید: برخی از شناساگرهای pH (مانند متیل اورانژ و برموتیمول بلو) در برابر نور تجزیه میشوند، بنابراین باید در ظروف تیره و در محیط خنک و خشک نگهداری شوند.
• نگهداری در ظروف دربسته: برای جلوگیری از تبخیر یا آلودگی محلولهای شناساگر.
• دور از مواد ناسازگار: برخی شناساگرها ممکن است در مجاورت مواد دیگر واکنش دهند. برای مثال، شناساگرهای حاوی الکل باید دور از حرارت و شعله نگهداری شوند.
• برچسبگذاری صحیح: نام ماده، غلظت و هشدارهای ایمنی روی ظروف نگهداری ثبت شود تا از اشتباهات جلوگیری شود.
⚠ هنگام تهیه و استفاده از محلولهای شناساگر:
• همیشه مقدار کمی از شناساگر را استفاده کنید: نیازی به استفاده از حجم زیاد نیست، زیرا حتی مقادیر کم هم تغییر رنگ را نشان میدهند.
• هرگز شناساگرها را با دست لمس نکنید: برخی از آنها (مانند فنل فتالئین) دارای ترکیبات سمی هستند.
• استفاده از پیپت یا قطرهچکان: برای انتقال محلولهای شناساگر، هرگز از وسایل غیرمجاز یا سرنگهای آلوده استفاده نکنید.
• مخلوط نکردن شناساگرهای مختلف بدون دانش کافی: ترکیب برخی شناساگرها ممکن است باعث تولید مواد سمی یا ناپایدار شود.
⚠ جلوگیری از استنشاق یا بلعیدن شناساگرها:
• هرگز شناساگرها را بو نکنید: برخی شناساگرها مانند تیمول بلو ممکن است بخارات تحریککننده تولید کنند.
• از خوردن و آشامیدن در محیط کار پرهیز کنید: ممکن است ذرات یا بخارات شناساگر وارد غذا یا نوشیدنی شوند و سلامتی را به خطر بیندازند.
• در صورت تماس با دهان یا بلعیدن: فوراً دهان را با مقدار زیادی آب شستشو دهید و با مرکز کنترل سموم یا پزشک تماس بگیرید.
⚠ ایمنی هنگام دفع و دور ریختن شناساگرها:
• هرگز محلولهای شناساگر را مستقیماً در سینک نریزید: برخی از آنها ممکن است باعث آلودگی محیط زیست شوند.
• دفع صحیح بر اساس دستورالعملهای زیستمحیطی: محلولهای حاوی فلزات سنگین (مانند برخی از شناساگرهای فلورسنت) باید در ظروف مخصوص مواد زائد شیمیایی جمعآوری شوند.
• ریختن محلولهای باقیمانده در ظروف زباله مخصوص: در آزمایشگاهها، ظروف جداگانه برای دفع مواد شیمیایی وجود دارد که باید مطابق با دستورالعملهای ایمنی استفاده شوند.
• در صورت نشت مواد، محیط را بلافاصله تمیز کنید: برای جلوگیری از آسیبهای پوستی یا آلودگی سایر تجهیزات.
⚠ رعایت نکات ایمنی در هنگام انجام آزمایشهای دانشآموزی:
• نظارت معلم یا مسئول آزمایشگاه الزامی است: هنگام استفاده از شناساگرها در مدارس و دانشگاهها، همیشه باید یک فرد آگاه حضور داشته باشد.
• استفاده از مقادیر بسیار کم: برای کاهش خطرات، بهویژه هنگام آزمایش با دانشآموزان.
• شناساگرهای طبیعی را جایگزین کنید: در صورت امکان، بهجای شناساگرهای شیمیایی از شناساگرهای طبیعی مانند آب کلم قرمز، چای سبز یا زردچوبه استفاده کنید.
⚠ اقدامات فوری در صورت بروز حادثه:
اگر به هر دلیلی فردی در تماس مستقیم با شناساگرها قرار گرفت، اقدامات زیر را انجام دهید:
• تماس با پوست: بلافاصله محل تماس را با مقدار زیادی آب بشویید و در صورت ایجاد التهاب، به پزشک مراجعه کنید.
• تماس با چشم: چشمها را حداقل ۱۵ دقیقه با آب سرد شستشو دهید و سریعاً به پزشک مراجعه کنید.
• استنشاق بخارات سمی: فرد را به محیط باز انتقال دهید و در صورت بروز مشکل تنفسی، فوراً اورژانس را خبر کنید.
• بلعیدن تصادفی: هرگز فرد را وادار به استفراغ نکنید؛ بلکه سریعاً مقدار زیادی آب بنوشد و کمک پزشکی دریافت کند.
جمعبندی
شناساگرهای اسید و باز (معرفهای pH) ابزارهای مهمی در علم شیمی هستند که با تغییر رنگ خود، میزان اسیدی یا بازی بودن یک محلول را مشخص میکنند. این مواد در آزمایشگاهها، صنایع دارویی، تصفیه آب، کشاورزی و بسیاری از حوزههای دیگر کاربرد دارند. برخی از آنها بهصورت شیمیایی تولید شدهاند، مانند متیل اورانژ و فنل فتالئین، و برخی دیگر بهطور طبیعی در گیاهانی مانند کلم قرمز و چای سیاه یافت میشوند.
انتخاب شناساگر مناسب، بسته به نوع اسید و باز موجود در محلول، اهمیت زیادی دارد؛ بهویژه در تیتراسیونها که نیاز به دقت بالایی دارند. همچنین در استفاده از این مواد باید نکات ایمنی را رعایت کرد تا از خطرات احتمالی جلوگیری شود.
برای بازدید از فروشگاه و سفارش شناساگرهای مختلف اسید و باز و سایر محصولات شیمیایی، کلیک کنید:





